チザニジンの作用機序と脊髄反射抑制・薬物動態を徹底解説
喫煙患者にチザニジンを処方すると、効果が約30%失われることがあります。
チザニジンの作用機序:α2受容体刺激と脊髄多シナプス反射の抑制

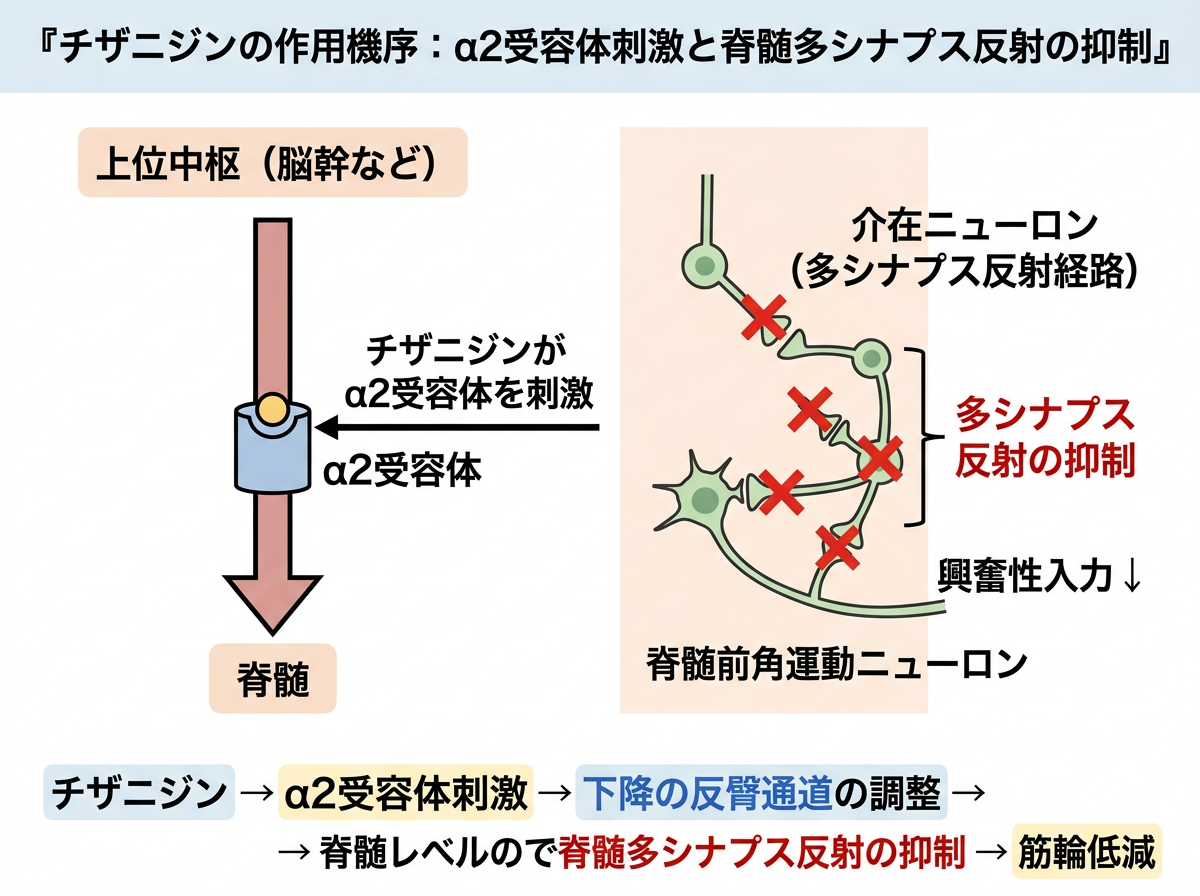
チザニジン(商品名:テルネリン)は、中枢性筋弛緩薬に分類される筋緊張緩和剤です。その核心にある作用機序は、「中枢性アドレナリンα2受容体の刺激」にあります。
チザニジンは脊髄および脊髄上位中枢に作用し、α2受容体を介して興奮性介在ニューロンからのノルアドレナリン放出を抑制します。これにより、シナプス前・シナプス後の双方で神経伝達が抑制され、骨格筋の過剰な緊張が解放されます。つまり、「過緊張の火元となる神経回路を中枢レベルで抑える」というアプローチです。
重要なのは、チザニジンが多シナプス反射を選択的に抑制するという点です。脊髄後根刺激による多シナプス反射電位は明確に抑制される一方、単シナプス反射電位への抑制は弱いことが動物実験(ラット・ネコ)で確認されています。これが基本です。
単シナプス反射は正常な筋収縮・姿勢維持に欠かせない反射であり、これを過度に抑制すると脱力や運動障害を引き起こします。病的な筋緊張亢進の多くは多シナプス経路を介しているため、チザニジンはそこを標的にすることで、正常な運動機能をできる限り温存しながら過緊張を和らげる設計になっています。
さらに、チザニジンにはγ運動ニューロンを抑制する作用もあります。筋紡錘(筋肉の緊張を感知するセンサー)を直接抑制するのではなく、脊髄からのγ運動ニューロン出力を抑制し、二次的に筋紡錘の感度を低下させます。これが過緊張の「フィードバックループ」を断ち切る仕組みです。意外ですね。
加えて、侵害刺激に対する脊髄後角ニューロンの興奮を抑制する「抗侵害受容作用」も確認されています(非侵害刺激への反応は抑制しない)。腰痛や頸肩腕症候群の痛みの軽減にも関与すると考えられており、単なる筋弛緩薬の枠を超えた薬理プロファイルをもっています。
| 作用 | 部位・機序 | 結果 |
|---|---|---|
| α2受容体刺激 | 脊髄・上位中枢 | 興奮性ニューロン抑制→筋緊張緩和 |
| 多シナプス反射抑制 | 脊髄後根経路 | 病的筋緊張の選択的解除 |
| γ運動ニューロン抑制 | 脊髄γ系路 | 筋紡錘感度の二次的低下 |
| 抗侵害受容作用 | 脊髄後角 | 疼痛シグナルの抑制 |
参考:添付文書の薬効薬理詳細(KEGG医薬品情報・添付文書)
KEGG医薬品情報:チザニジン錠1mg「JG」添付文書(薬効薬理・18条)
チザニジン作用機序の土台:α固縮・γ固縮モデルと実験的根拠
チザニジンの筋弛緩作用は、動物実験における「除脳固縮モデル」で体系的に検証されています。α2受容体刺激薬としての位置づけを理解するうえで、この実験的背景は薬剤師・医師いずれにとっても有用な知識です。
除脳固縮には大きく2種類あります。「α固縮(貧血性除脳固縮)」と「γ固縮(上丘・下丘間除脳固縮)」です。チザニジンはラット実験において、この両方の固縮モデルを緩解することが確認されています(Ono H. et al., Gen. Pharmac., 1986)。
α固縮は主に α運動ニューロン(骨格筋を直接支配するニューロン)の過活動によるもので、γ固縮はγ運動ニューロンを介した筋紡錘からのフィードバック亢進によるものです。チザニジンがこの双方に有効であるのは、α2受容体を介した広域的な脊髄抑制機序を持つためです。これは使えそうです。
また、多シナプス反射の一種である「脚の交差性伸展反射」を抑制することもヒヨコを用いた実験で示されています。交差性伸展反射は痛み刺激などに応じて起こる複雑な反射であり、それが抑制されることは、痙性麻痺や慢性疼痛への効果を裏付ける実験的エビデンスとなっています。
エペリゾン(ミオナール)など他の中枢性筋弛緩薬と異なる点も整理しておきましょう。エペリゾンはγ系を中心とした抑制に加え血管拡張作用を持つのに対し、チザニジンはα2受容体作動による中枢性の脊髄反射抑制を主体とします。両者の使い分けは、副作用プロファイルや患者背景に依存します。
- チザニジン:α2受容体刺激、多シナプス反射の選択的抑制、痙性麻痺・筋緊張の双方に適応、CYP1A2代謝(相互作用に注意)
- エペリゾン:γ系抑制+血管拡張、筋血流改善、比較的副作用が少ないとされ、外来での筋緊張改善用途に頻用
- バクロフェン:GABA-B受容体作動、脊髄性の強い痙性麻痺(多発性硬化症等)に有効、副作用に眠気・筋力低下
適応疾患と薬剤選択の判断軸を知ることで、処方設計の精度が上がります。
チザニジンの薬物動態:CYP1A2代謝と喫煙・禁煙が引き起こす意外な落とし穴
チザニジンは経口投与後に吸収され、主として肝臓の代謝酵素「CYP1A2」によって代謝されます。半減期は約1.5時間と短く、食後投与が基本です。CYP1A2代謝が主経路である点が、この薬の多くの相互作用と副作用リスクを生み出しています。
ここで多くの医療従事者が見落としがちな事実があります。喫煙患者への処方時、チザニジンのAUC(血中濃度-時間曲線下面積)が非喫煙者と比べて約30%低下するという報告があります。タバコの煙に含まれる多環芳香族炭化水素がCYP1A2を誘導し、チザニジンの代謝を亢進させるためです。
つまり「喫煙者にチザニジンを処方しても、血中濃度が期待通りに上がらず効果が出にくい」可能性があるということです。これが条件です。
さらに注意すべきは「禁煙時」です。禁煙によってCYP1A2の誘導が解除されると、それまで低めに抑えられていたチザニジンの血中濃度が一気に上昇します。用量調節なしに継続投与していると、眠気・血圧低下・ふらつきが増強するリスクが生じます。入院中に禁煙指導を行う際などは、チザニジンを服用中でないか確認する習慣をもつことが大切です。
また、リファンピシン(抗結核薬)もCYP1A2誘導薬であり、チザニジンとの併用でAUCが50%低下する報告があります。結核治療中の患者への処方では特に注意が必要です。
腎機能低下がある患者でも排泄遅延による血中濃度の高値持続が起こるため、高齢者や腎障害患者への投与では減量を検討します。高齢者への注意が原則です。
| 要因 | CYP1A2への影響 | チザニジンへの影響 |
|---|---|---|
| フルボキサミン(SSRI) | 強力な阻害 | AUC最大33倍↑(併用禁忌) |
| シプロフロキサシン | 阻害 | AUC約10倍↑(併用禁忌) |
| 喫煙(1日10本超) | 誘導 | AUC約30%↓(効果減弱) |
| リファンピシン | 誘導 | AUC約50%↓(効果減弱) |
| 経口避妊薬・チクロピジン | 阻害 | 血中濃度上昇・副作用増強のおそれ |
参考:チザニジンのCYP1A2相互作用に関する情報
民医連:副作用モニター情報〈292〉テルネリン(塩酸チザニジン)とフルボキサミンの相互作用
チザニジンの重大な副作用:血圧低下・肝機能障害・ショックへの対応
チザニジンは筋緊張緩和薬として広く使われていますが、重大な副作用を見逃さないことが医療安全の観点から非常に重要です。添付文書が定める「重大な副作用」は計5項目あります。
最もリスクが高いのが「ショック」と「急激な血圧低下」です。チザニジンは中枢性α2刺激作用を持つため、血圧低下は作用機序に根ざした副作用です。特に高齢者や降圧薬を併用している患者では、投与開始初期に著明な血圧低下が起こりやすいとされています。急激な血圧低下には期限があります——投与開始直後が最も危険です。
「心不全」(心拡大・肺水腫等)や「呼吸障害」(喘鳴・喘息発作・呼吸困難)の報告もあり、いずれも頻度不明ながら、発現時は直ちに投与を中止し適切な処置が必要です。
「肝炎・肝機能障害・黄疸」も重大な副作用に含まれます(頻度不明)。AST・ALTの著しい上昇、悪心・嘔吐、全身倦怠感などが初期症状として現れます。また、0.1〜5%未満の頻度でAST・ALTの軽度な上昇も報告されており、定期的な肝機能チェックが望まれます。チザニジンは重篤な肝障害のある患者には禁忌である点も忘れてはなりません。
痛いところは、「頻度不明」という記載が多い点です。頻度不明だから安全、ではありません。市販後の症例報告からリストされた項目であり、実際の発現率は定義上評価できないことを意味します。
その他の副作用(0.1〜5%未満)では眠気・めまい・ふらつき・血圧低下・口渇・悪心などが主体です。高齢者での転倒リスクを念頭に、初回処方時から患者への説明を丁寧に行うことが求められます。患者が安心できる説明が基本です。
- ショック・急激な血圧低下:顔面蒼白、冷汗、意識消失など。特に高齢者と降圧薬併用時に注意。
- 心不全:心拡大・肺水腫の報告あり。息切れや浮腫の急激な悪化に注意。
- 呼吸障害:喘鳴・喘息発作・呼吸困難が出現したら即中止。
- 肝炎・肝機能障害・黄疸:全身倦怠感・皮膚黄染などが出現した際は速やかに肝機能検査を実施。
参考:チザニジンの副作用・添付文書情報(日経メディカル)
日経メディカル:チザニジン錠1mg「サワイ」基本情報・副作用一覧
チザニジンの適応と用量設定——筋緊張状態と痙性麻痺で投与戦略が変わる独自視点
チザニジンの添付文書上の適応は、大きく2カテゴリに分かれます。「筋緊張状態の改善」と「痙性麻痺の治療」です。この2つは同じ薬剤の適応でありながら、用量設定の戦略がまったく異なります。この違いを意識せずに一律で処方すると、効果不十分や副作用過多のどちらかに陥るリスクがあります。
まず「筋緊張状態の改善」(頸肩腕症候群・腰痛症など)では、通常1日3mg(1mgを1日3回、食後)が標準用量です。臨床試験では「中等度改善以上が57.9%(2週後)」という結果が得られており、1〜2週間での効果発現を見ながら継続を判断します。これが原則です。
一方、「痙性麻痺」(脳血管障害・外傷後遺症・多発性硬化症など)では、1日3mgから開始し、効果を確認しながら1日6〜9mgへ漸増するアプローチをとります。痙性麻痺は筋緊張が非常に強い状態であることが多く、より高用量が必要になることがあります。ただし、用量を増やすほど副作用(血圧低下・眠気)のリスクも上がります。増量には慎重な観察が条件です。
臨床的に重要なもう一つのポイントは「飲み合わせの全体像」です。筋緊張や痙性麻痺を持つ患者は、降圧薬、睡眠薬、中枢神経抑制薬を同時に処方されているケースが多くあります。チザニジンとこれらの薬剤を組み合わせると、低血圧・過鎮静・転倒リスクが相加的に高まります。特に高齢者では、ポリファーマシー(多剤併用)の文脈でチザニジンの必要性を随時見直すことが求められています。
また「動物実験(サル)により精神依存の形成が示唆された」との記載が添付文書の「その他の注意」にあります。長期投与する際の漫然継続を避け、症状の改善に応じて減薬・中止を検討する習慣が適切な使用法です。
処方設計を考える際には、「どの適応で使うか」「患者の腎・肝機能は?」「禁煙・喫煙の状況は?」「CYP1A2を阻害する薬剤が処方されていないか?」という4つの視点を毎回チェックする流れを作ることで、安全性と有効性の両立を図ることができます。これだけ覚えておけばOKです。
| 区分 | 代表疾患 | 開始用量 | 維持・最大用量 |
|---|---|---|---|
| 筋緊張状態の改善 | 頸肩腕症候群、腰痛症 | 1日3mg(分3) | 症状に応じて適宜増減 |
| 痙性麻痺 | 脳血管障害、脊髄損傷後遺症、多発性硬化症など | 1日3mgから開始 | 漸増し1日6〜9mgまで(分3) |
参考:チザニジンの適応・用量・使い分けに関する詳細
薬局業務NOTE:エペリゾンとチザニジンの違い・痙性麻痺における用量比較
