レザルタス ジェネリックの現状と選択肢を徹底解説
レザルタスのジェネリックは「もう出ている」と思い込んでいると、患者の薬代が毎月1,200円以上余分にかかり続けます。
レザルタスとは何か:ARB配合剤としての薬効と特徴

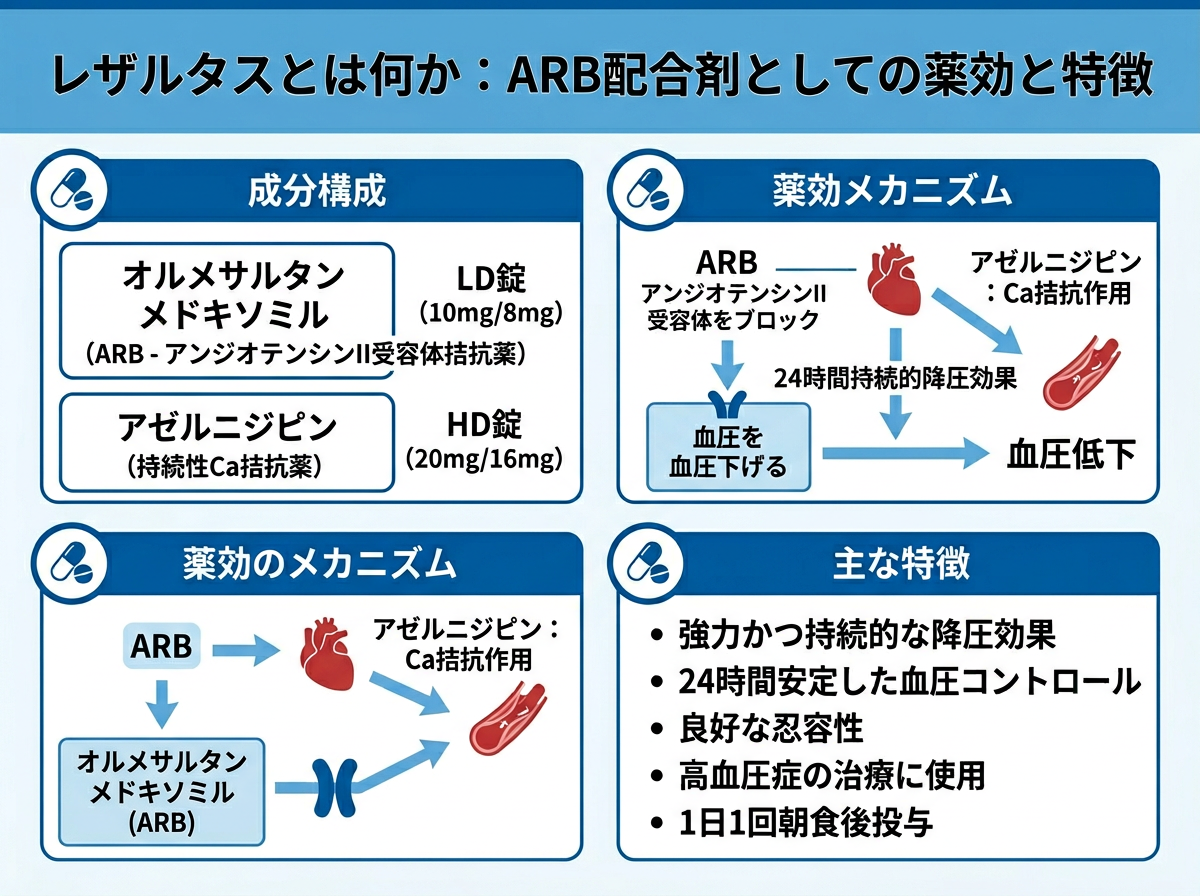
レザルタス配合錠は、第一三共が2010年に発売したARB(アンジオテンシンII受容体拮抗薬)と持続性Ca拮抗薬の配合剤です。正式な一般名は「オルメサルタン メドキソミル・アゼルニジピン配合剤」で、ARB成分のオルメサルタン メドキソミルとCa拮抗薬成分のアゼルニジピンを1錠にまとめた高血圧症治療薬です。
規格はLD(Low Dose)とHD(High Dose)の2種類があります。具体的な含量は以下の通りです。
| 規格 | オルメサルタン量 | アゼルニジピン量 | 薬価(2026年時点) |
|------|----------------|----------------|-------------------|
| LD(低用量) | 10mg | 8mg | 25.80円/錠 |
| HD(高用量) | 20mg | 16mg | 48.00円/錠 |
LDからHDへ変更する際は両成分が同時に倍量になる点が特徴で、他のARB/CCB配合剤(例:ミカムロ配合錠はテルミサルタンのみ増量)とは異なります。これは処方変更時に必ず確認すべきポイントです。
用法は1日1回1錠を朝食後経口投与。「本剤は高血圧治療の第一選択薬として用いない」という規定があり、原則としてオルメサルタンとアゼルニジピンを既に併用中もしくはいずれか一方で血圧コントロールが不十分な患者への切り替えを検討する薬です。ここは条件がある点です。
アゼルニジピンは主にCYP3A4で代謝されるため、イトラコナゾールをはじめとするアゾール系抗真菌薬やHIVプロテアーゼ阻害薬との併用禁忌があります。2024年8月にはポサコナゾール(ノクサフィル)との禁忌も追加された点は要注意です。薬歴確認の際に見落とされやすい組み合わせの1つと言えます。
参考:PMDAによるレザルタス配合錠の添付文書情報(2025年9月改訂版)は医療関係者向けに以下で参照できます。
PMDA 医療用医薬品情報(医療関係者向け)- レザルタス配合錠LD/HD
レザルタス ジェネリックが存在しない現状と背景
2026年3月現在、レザルタス配合錠LD・HDのいずれにも後発品(ジェネリック医薬品)は薬価収載されていません。後発品なしの先発品のみという状態が続いています。
なぜ後発品がないのか、という疑問は多くの医療従事者が持つところです。実は経緯があります。
第一三共のジェネリック医薬品子会社「第一三共エスファ」は、2017年2月にレザルタス配合錠のAG(オーソライズドジェネリック)の製造販売承認を取得していました。AGとは、先発品メーカーの許諾を得て同一の原薬・添加物・製造方法で製造されるジェネリック医薬品です。しかしこのAGは、同年6月の薬価追補収載を見送り、その後も薬価基準に収載されないままとなっています。
当時の報道によれば、第一三共グループとしてはオルメテック(オルメサルタン単剤)のAGを先行させる戦略を取り、レザルタスのAGは優先順位が後回しになったとされています。配合剤という複雑な製剤であることも収載手続きのハードルを上げた要因の一つです。
その後、後発品専業メーカーからの収載申請も現時点では確認されておらず、同一成分(オルメサルタン+アゼルニジピン)の後発品は市場に存在しません。つまり、後発品がないのは特許の問題だけではなく、事業戦略的な判断も絡んでいます。
医療現場において、「レザルタスにジェネリックを出してください」という患者からの希望に応えられないのが現状です。この事実は薬局や病院薬剤師、処方医双方が共有しておく必要があります。
データインデックス:レザルタス配合錠LDの先発品・後発品(ジェネリック)検索(後発品なしを確認)
選定療養制度との関係:後発品なしはどう扱われるか
2024年10月から始まった長期収載品の選定療養制度は、医療現場に大きなインパクトを与えました。ここでは、レザルタス配合錠がどのような扱いになるのかを整理します。
選定療養の対象となるのは「後発医薬品が存在する先発医薬品(長期収載品)」です。レザルタス配合錠は後発品が存在しないため、この制度の対象外となります。
つまりこういうことです。患者がレザルタス配合錠を希望して服用し続けても、「特別の料金(先発品と後発品の価格差の1/4)」を追加で自己負担させる制度は適用されません。後発品がない先発品である限り、通常の保険給付が維持されます。
これは一見プラスに映りますが、裏返せば「コスト削減の手段が限られている」ことも意味します。後発品があれば選定療養の対象になる一方で、患者がジェネリックに変更すれば薬剤費が下がります。しかしレザルタス配合錠の場合は選択肢そのものがない状態です。
一方で注意すべき点があります。制度変更は随時行われます。厚生労働省は2026年4月にも選定療養対象品目の見直しを実施しており、収載状況は常に流動的です。今後レザルタスのAGや後発品が収載された際には、即座に選定療養の対象品目となる可能性があります。
薬剤師や医師として重要なのは、現時点での収載状況を定期的に確認する習慣を持つことです。医薬品データベース(データインデックス、KEGGメドラスなど)での定期チェックが実務上の対応策になります。
長野県保険医協会:2026年4月1日からの長期収載品に係る選定療養の対象医薬品変更情報
単剤後発品への切り替えで患者の薬代を下げる実務的戦略
レザルタス配合錠自体のジェネリックはないものの、配合されている2成分はそれぞれ単剤での後発品が存在します。この事実は実務において非常に重要です。
オルメサルタン メドキソミルの後発品(オルメテックのジェネリック)は既に多数のメーカーから発売されており、例えばオルメサルタンOD錠20mg「JG」の薬価は1錠20.2円です(先発品オルメテックOD錠20mgは25.4円)。アゼルニジピンの後発品(カルブロックのジェネリック)については現時点での発売状況の確認が必要ですが、成分として市場に選択肢があります。
レザルタス配合錠HD(オルメサルタン20mg+アゼルニジピン16mg)の薬価は1錠48.00円です。30日分で1,440円(10割)、3割負担なら432円が薬剤費部分の自己負担です。これを単剤後発品2種類の組み合わせに切り替えることができれば、月単位では数百円、年単位では数千円規模の削減につながる可能性があります。
ただし重要な注意点があります。配合剤から単剤への切り替えは、処方変更が必要です。薬剤師が勝手に行うことはできず、医師への情報提供・疑義照会を通じて処方変更してもらう形になります。また、患者によっては配合剤の服薬本数削減効果(アドヒアランス維持)を優先すべきケースもあります。コスト削減と服薬継続率のバランスを個々の患者ごとに判断することが条件です。
実際に処方医への情報提供を検討する際は、「患者さんのご希望でコスト削減を検討しています。オルメサルタンおよびアゼルニジピンの単剤後発品への変更は可能でしょうか」という形で具体的に提案するのが実務上スムーズです。患者の同意を必ず事前に確認しておきましょう。
レザルタス ジェネリックへの切り替えを検討する際の注意事項と実務チェックリスト
将来的にレザルタスのジェネリックが収載された際、あるいは現時点で単剤後発品への切り替えを検討する際に確認すべき実務的なポイントをまとめます。
まず薬剤学的な確認事項として、レザルタス配合錠はLDとHDで成分量が2倍異なるため、切り替え先の規格を誤ると投与量が2倍になるリスクがあります。ミカムロ配合錠のようにCa拮抗薬のみ増量されるものとは異なり、両成分が同時に倍量になる点は特に注意が必要です。
次に、禁忌・相互作用の再確認も欠かせません。
- ✅ アゾール系抗真菌薬(イトラコナゾール、ミコナゾール、フルコナゾール、ボリコナゾール、ポサコナゾールなど)の併用の有無
- ✅ HIVプロテアーゼ阻害薬(リトナビル含有製剤、ダルナビルなど)・コビシスタット含有製剤の有無
- ✅ 新型コロナ治療薬のニルマトレルビル・リトナビル(パキロビッド)、エンシトレルビル(ゾコーバ)との関係(追加収載が2024年以降に相次いでいる)
- ✅ シンバスタチン・シクロスポリン(AUCが約2倍に上昇するとの報告あり)
- ✅ 妊婦・妊娠の可能性がある女性(ARBとして禁忌)
特に、新型コロナ治療薬との禁忌は近年の追記事項です。外来で高血圧患者が新型コロナに罹患した際に生じる場面を想定しておくことが大切です。
切り替え後のフォローアップも実務では重要です。同一成分への後発品切り替えとはいえ、添加物の違いにより稀に患者が体感の違いを訴えるケースがあります。切り替え後1〜2週間以内に血圧測定値や自覚症状に変化がないかを患者自身に確認してもらうよう伝えておくことが丁寧な対応につながります。
処方変更後は必ずレセプト上の記載確認も行いましょう。配合剤から2種の単剤に変更した場合、薬剤数の変化が加算要件に影響する可能性があります。施設のルールに沿って対応することが原則です。
厚生労働省:処方せんに記載された医薬品の後発医薬品への変更について(変更調剤ルールの基本通知)
独自視点:配合剤のジェネリック収載遅延が医療現場に与える構造的課題
「配合剤にはなかなかジェネリックが出ない」という現象は、レザルタスに限った話ではありません。これは日本の後発医薬品市場が抱える構造的な課題と深く結びついています。
後発品専業メーカーにとって、配合剤の後発品申請は単剤と比べてハードルが高くなります。生物学的同等性試験を2成分それぞれで実施しなければならず、開発コストが単剤の倍近くかかります。加えて、先発品メーカーがAGを事実上「温存」することで、独立した後発品メーカーの市場参入が後手に回る状況も生まれています。
国としては後発品の数量シェア目標(2023年度末までに80%以上)を掲げていましたが、配合剤の収載遅延は目標達成の「抜け穴」になり得るという指摘もあります。特に服薬アドヒアランスを高めるための配合剤処方が増える中で、その後発品が出ないとなれば患者の薬剤費削減効果が限定されます。これは医療財政の観点からも注視すべき点です。
薬剤師・医師として対応できることは、①現在の収載状況を定期的にモニタリングする、②患者への説明時に「現時点でジェネリックはない」と明確に伝える、③後発品が収載され次第迅速に情報提供できる準備をしておく、の3点に集約されます。
後発品収載の最新情報は厚生労働省の薬価基準収載品目リストや、医薬品データベースで随時確認できます。年2回(4月・10月)の薬価改定と随時の追補収載のタイミングでの確認が実務上の基本です。
日本ジェネリック製薬協会:6月追補 初後発品15成分、うちAGは2成分(レザルタス収載状況を含む背景情報)
内閣府経済財政諮問会議:後発品未収載の先発品一覧(レザルタス配合錠HDが記載)- 2025年4月

【指定医薬部外品】新ビオフェルミンSプラス錠 550錠 61日分 大正製薬 整腸剤 [乳酸菌/ビフィズス菌/ロンガム菌/フェーカリス菌/アシドフィルス菌 配合] 腸内フローラ改善 便秘や軟便に