ジャヌビア錠50mgジェネリックの承認・薬価・処方注意点
承認済みの後発品でも、特許訴訟が継続する限り薬価収載は見送られ続けます。
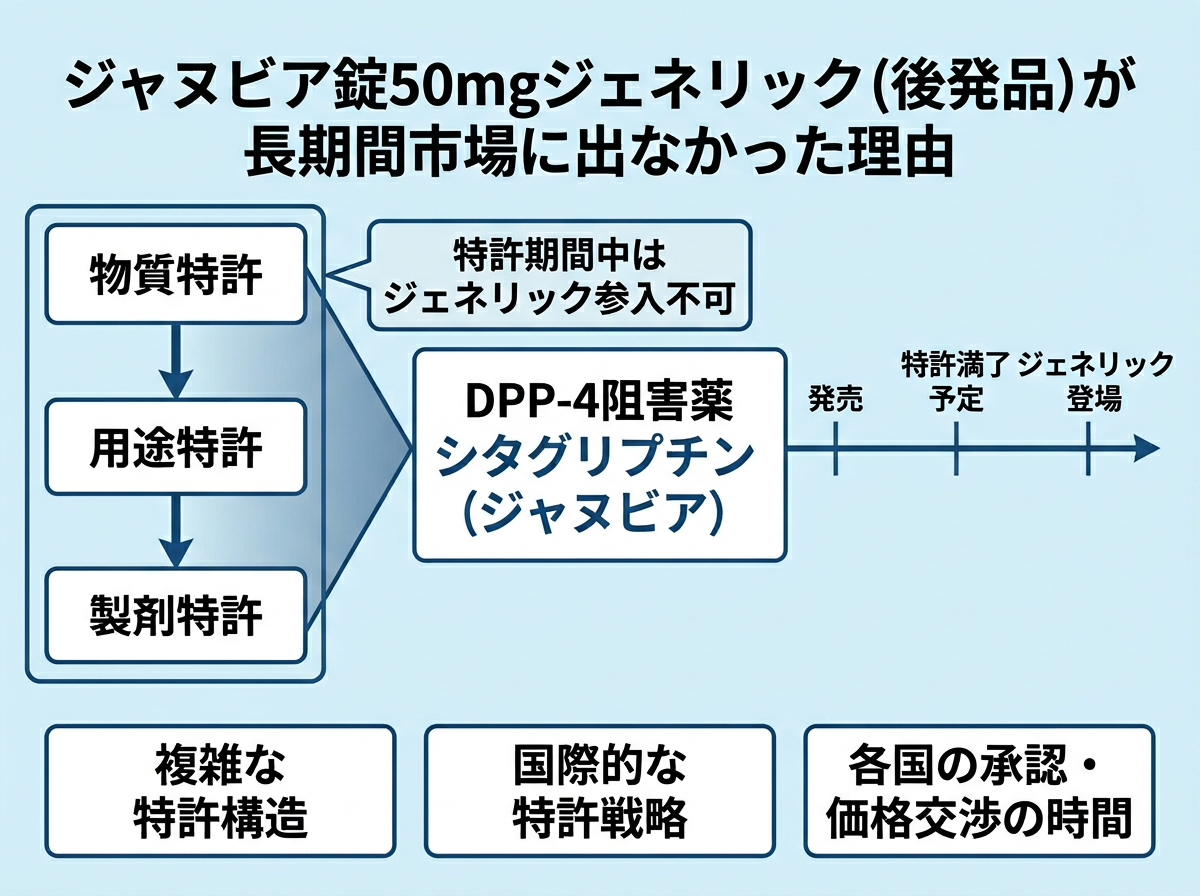
ジャヌビア錠50mgジェネリック(後発品)が長期間市場に出なかった理由

ジャヌビア錠(一般名:シタグリプチンリン酸塩水和物)は、MSD株式会社が製造販売するDPP-4阻害薬です。2009年12月に国内初のDPP-4阻害薬として発売され、2型糖尿病治療における中心的な薬剤として長年使用されてきました。
「後発品が出ていないのはまだ特許が続いているからでは?」と思っていた方も多いかもしれません。実際はそれだけではありませんでした。
シタグリプチンの物質特許(特許第3762407号)の本来の満了日は2022年7月5日でした。しかし、「ジャヌビア®錠」の承認に基づき特許存続期間の延長登録が行われ、効能・効果ごとに2025年2月21日〜2026年3月30日まで延長されていました。
この延長特許が残っている2023年8月、サワイグループホールディングスの子会社であるメディサ新薬がいち早くジャヌビア後発品として「シタグリプチン錠『サワイ』」の承認を取得しました。しかし同製品の有効成分は「シタグリプチンリン酸塩(無水物)」であり、先発品の「水和物」とは形態が異なっていました。
つまり、「水和物と無水物は別成分だから延長特許は及ばない」という解釈でパテントリンケージをくぐり抜けて承認された形です。意外ですね。
これに対しMSD側は2023年10月に特許権侵害訴訟および差止仮処分命令申立てを東京地方裁判所に提起。結果として約2年以上の審理を経て、2026年2月3日に沢井製薬らがMSDの主張をすべて認諾し訴訟が終結しました。延長特許の効力は水和物・無水物の差異を超えて後発品にも及ぶとのMSD側の立場が全面的に認められた形です。
この訴訟継続期間中、2023年12月の後発品薬価追補収載でもシタグリプチン後発品は収載が見送られています。特許問題があるうちは収載が難しいという実態が浮き彫りになった事例です。これが原則です。
別の動きとして、2025年2月17日には第一三共エスファが「シタグリプチンリン酸塩錠『DSEP』(12.5mg/25mg/50mg/100mg)」の承認を取得しました。こちらはAG(オーソライズドジェネリック)の可能性が業界では高いと見られています。
特許の最終満了日である2026年3月30日を経て、今後は複数の後発品メーカーが本格的に薬価収載を目指す見通しです。日刊薬業(2026年1月)の報道によると、後発品各社が2026年の薬価追補収載ターゲットにジャヌビアを明確に据えているとのことです。
参考リンク(ジャヌビア後発品の特許訴訟終結に関する詳細)。
沢井がMSDの主張を全面認諾する形で終結 — 延長特許権の効力と水和物/無水物の評価(特許戦略ブログ)
ジャヌビア錠50mgジェネリックの薬価と医療費への影響
先発品の現在の薬価を確認しておきましょう。ジャヌビア錠50mgは82.1円/錠(2024年改定後)です。1日1回服用として30日分の薬剤費は2,463円になります。年間換算(365日)では約30,000円を患者が支払う費用の基礎となっています。
後発品の薬価はどうなるでしょうか?後発品の薬価算定ルールでは、初めて後発品が市場に登場する場合、基本的に先発品の薬価の約5割(50%)程度に設定されます。仮に50%に設定されるなら約41円/錠となり、1日1回30日分では約1,230円。これは患者の自己負担削減にも直結します。
3割負担の患者であれば、先発品の月あたり自己負担が約739円、後発品では約369円程度となります。年間で概算すると約4,400円〜8,800円の差が生まれる可能性があります。これは使えそうです。
医療機関・薬局にとっても、後発品使用体制加算の算定要件(後発品調剤率75%以上など)を維持する観点から、使用数の多いDPP-4阻害薬のシタグリプチン後発品が収載されることは意義が大きいと言えます。
また、2025年6月の追補収載でシタグリプチン後発品(エスファ品)は収載見送りとなっています。これは当時まだ特許訴訟が進行中であったことが主な理由です。2026年3月30日の特許最終満了後、次の追補収載(6月または12月)での登場が現実的なラインと見られています。
参考リンク(後発品薬価算定ルールの解説)。
後発医薬品の薬価決定ルール(Japan Health Policy NOW)
ジャヌビア錠50mgジェネリックと腎機能別の用量設定ポイント
シタグリプチンは主として腎臓から未変化体として排泄される腎排泄型薬剤です。ここが処方の際に最も注意を要するポイントです。
後発品に切り替えても、薬効・用量設定のルールは先発品と同様です。腎機能に応じた用量調節が必要なことを忘れずに確認してください。
添付文書上の用量設定は以下のとおりです。
| 腎機能の区分 | eGFR(目安) | 推奨用量(シタグリプチンとして) |
|---|---|---|
| 正常〜軽度低下 | ≧45 mL/min/1.73m² | 50mg 1日1回(通常用量) |
| 中等度低下 | 30〜45 mL/min/1.73m² | 25mg 1日1回 |
| 高度低下〜末期腎不全 | <30 mL/min/1.73m² | 12.5mg 1日1回 |
高齢者糖尿病患者では腎機能低下が進行していることが多いため、「50mgで長く処方していたが実は腎機能が低下していた」という見落としリスクがあります。これは注意すべき点ですね。
とくに先発品から後発品への切り替えを検討する際、直近の血清クレアチニン値やeGFRの確認をルーティンに行うことが大切です。腎機能確認が条件です。
薬局でのヒヤリハット事例でも「腎機能低下患者に通常量50mgのシタグリプチンが処方継続されていた」ケースが報告されています(リクナビ薬剤師「腎機能低下者に通常用量でシタグリプチンが処方」事例)。後発品へ切り替えるタイミングは、腎機能の再評価を行う好機と位置づけると良いでしょう。
参考リンク(腎機能低下患者へのシタグリプチン処方事例)。
腎機能低下者に通常用量でシタグリプチンが処方(リクナビ薬剤師 ヒヤリ・ハット事例)
ジャヌビア錠50mgジェネリックへの切り替え時に確認すべき副作用と安全性
ジャヌビア錠(シタグリプチン)の後発品は、有効成分の薬理作用が先発品と同等であることが前提です。つまり、先発品で注意が必要な副作用は後発品でも同様に注意が必要です。副作用への備えは必須です。
⚠️ 重大な副作用(見逃しに注意)
| 副作用 | 主な症状の目安 |
|---|---|
| 急性膵炎 | 持続する激しい腹痛・嘔吐・発熱 |
| 間質性肺炎 | 空咳・息切れ・発熱 |
| 腸閉塞(イレウス) | 腹部膨満・嘔吐・排便停止 |
| 低血糖 | 発汗・動悸・意識障害(SU薬・インスリン併用時に注意) |
| 横紋筋融解症 | 筋肉痛・脱力・褐色尿 |
| 水疱性類天疱瘡 | 皮膚の大きな水疱・掻痒感 |
| 肝機能障害・黄疸 | 倦怠感・食欲不振・黄疸 |
急性膵炎については、DPP-4阻害薬全体でリスクが指摘されてきた副作用です。膵炎の既往がある患者への投与は慎重に行う必要があります。
水疱性類天疱瘡はやや見落とされがちな副作用です。高齢者に多く、皮膚科受診先でシタグリプチン使用が見過ごされることがあります。皮膚科からの問い合わせや、患者の皮膚症状の変化には丁寧に対応する姿勢が求められます。
間質性肺炎については、PMDAの医薬品リスク管理計画書にも「因果関係の否定できない国内副作用症例を集積したため設定した」と明記されています。乾性咳嗽が続く患者では早めに画像評価を検討することが賢明です。
通常の血糖降下薬に比べ、単独使用では低血糖リスクが低いとされるシタグリプチンですが、インスリン分泌促進薬(SU薬、グリニド系)やインスリン製剤との併用では低血糖が起こりうる点は見落としてはなりません。これが基本です。
参考リンク(ジャヌビアの医薬品リスク管理計画書・PMDA)。
ジャヌビア錠100mgに係る医薬品リスク管理計画書(PMDA)
ジャヌビア錠50mgジェネリックと先発品「グラクティブ」の関係——見落とされやすい重複投与リスク
これはあまり話題にならない視点ですが、実臨床で実際に発生した重大なインシデントです。
ジャヌビア(MSD)とグラクティブ(小野薬品)は、どちらも有効成分はシタグリプチンリン酸塩水和物でまったく同一の薬剤です。2009年のDPP-4阻害薬最初の承認から、「2社同時発売」という形で国内市場に投入されました。
複数の医療機関を受診している患者において、片方の医療機関でジャヌビア錠を処方され、別の医療機関でグラクティブ錠を処方されるという「同成分の重複処方」が実際に発生しています。これはお薬手帳確認の不備で起きやすいパターンです。薬剤師が処方箋を確認した際に「ジャヌビア錠とグラクティブ錠が同時に出ていた」ヒヤリハット事例が複数報告されています。
後発品が登場すると、さらに「シタグリプチン錠」という銘柄名でも流通するため、医師・薬剤師ともに同一成分の薬剤が3パターンの商品名(ジャヌビア・グラクティブ・後発品各種)で存在することを意識する必要があります。痛いですね。
後発品への切り替え対応を行う際は、患者のお薬手帳やレセプト情報に「グラクティブ(または後発品のシタグリプチン)が他院で出ていないか」を必ず確認するステップを組み込むことを強く推奨します。なぜなら、シタグリプチンの重複投与は過剰な血糖降下リスクだけでなく、副作用頻度の増加にもつながりうるからです。
電子お薬手帳アプリや、医療機関・薬局間での情報共有ツール(電子処方箋システムなど)を活用してこのリスクを減らすことが、これからの医療従事者に求められる実践的なアクションです。
参考リンク(ジャヌビアとグラクティブの重複処方ヒヤリハット事例)。
グラクティブ錠とジャヌビア錠が同時に処方されていた(リクナビ薬剤師)
