ダーブロック添付文書PDFで押さえる警告・用量調節・相互作用の重要注意点
4週ごとに増量していると、切替え後の透析患者でHb値が想定外に下がり患者クレームになることがあります。
ダーブロック添付文書PDFの入手方法と最新版の確認

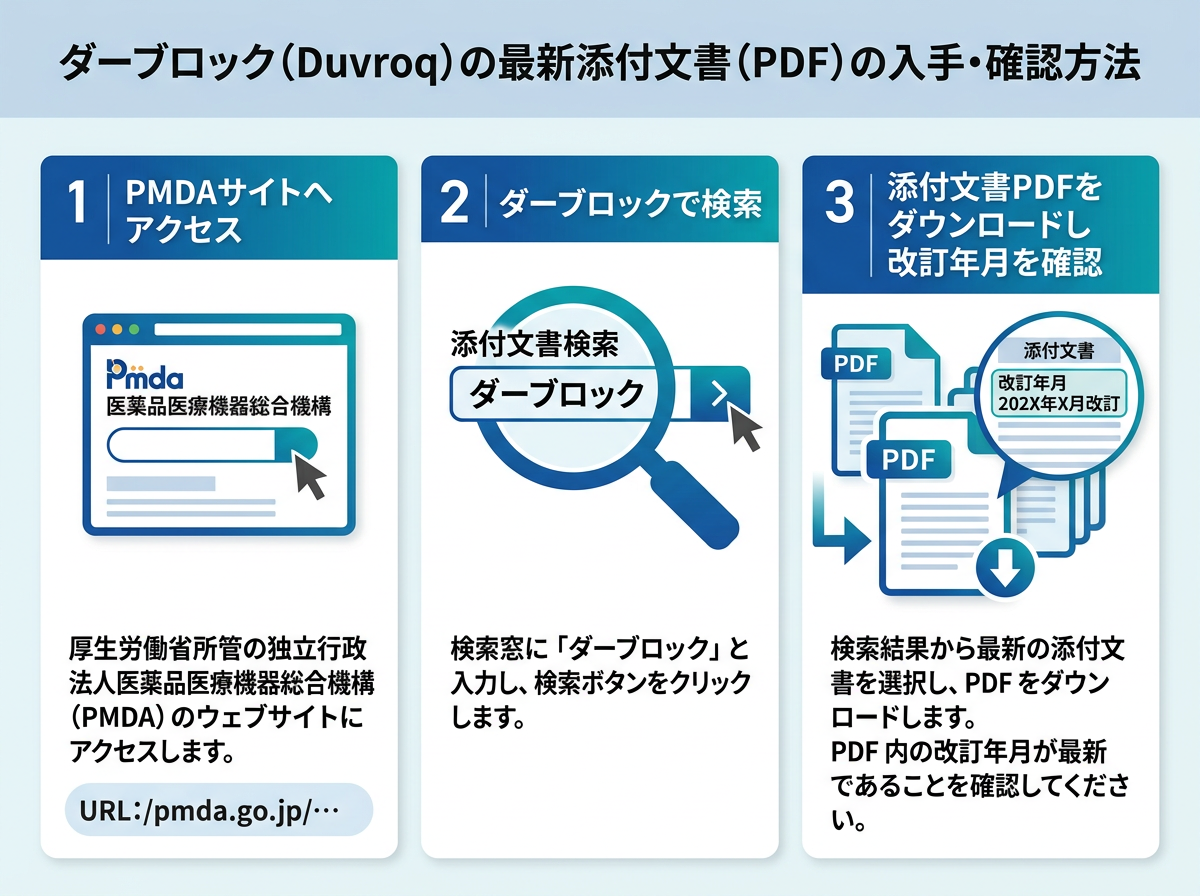
ダーブロック(一般名:ダプロデュスタット)の添付文書PDFは、PMDAの医療用医薬品情報検索ページから無料で入手できます。2026年3月時点の最新版は2024年7月改訂(第4版)であり、以前のバージョンと内容が一部異なるため、古い印刷物をそのまま使い続けるのは避けてください。
具体的な確認手順は、PMDAのサイトにアクセスし、「ダーブロック錠」で製品名を検索するだけです。1mg・2mg・4mg・6mgの各規格ごとにPDFが提供されており、内容はどの規格も共通です。インタビューフォーム(IF)は2025年7月に第6版が改訂されており、添付文書に記載されない詳細な薬物動態・調剤情報が網羅されています。
臨床現場では添付文書の改訂を見落とすリスクがあります。協和キリン株式会社が提供するくすり相談窓口(0120-850-150)を活用することも一つの選択肢です。最新情報は常にPMDAのページで確認するのが基本です。
製品の基本情報を整理すると以下のとおりです。
| 項目 | 内容 |
|---|---|
| 販売名 | ダーブロック錠 1mg / 2mg / 4mg / 6mg |
| 一般名 | ダプロデュスタット(Daprodustat) |
| 製造販売元 | グラクソ・スミスクライン株式会社(販売:協和キリン) |
| 販売開始 | 2020年8月 |
| 規制区分 | 劇薬・処方箋医薬品 |
| 効能・効果 | 腎性貧血 |
| 最新添付文書 | 2024年7月改訂(第4版) |
最新の添付文書はPMDAの公式サイトから確認できます。
ダーブロック添付文書PDFの警告と禁忌を正しく読む
添付文書の中で最も重要な項目の一つが「警告」です。ダーブロックには明確な警告が設定されており、医療従事者が投与前に必ず確認すべき内容が書かれています。
🔴 警告の要旨(添付文書 第1項)
本剤投与中に、脳梗塞・心筋梗塞・肺塞栓等の重篤な血栓塞栓症があらわれ、死亡に至るおそれがあるとされています。投与開始前には、これらの合併症や既往歴の有無を含めた血栓塞栓症のリスクを評価した上で、投与の可否を慎重に判断することが求められています。
臨床試験での血栓塞栓症の発現頻度は0.8%と報告されています。内訳は脳梗塞0.3%、肺塞栓症0.3%、網膜静脈閉塞0.3%、深部静脈血栓症0.3%です。頻度は低くみえますが、死亡に至る可能性がある重篤な副作用です。
禁忌は原則として1点のみで、「本剤の成分に対し過敏症の既往歴のある患者」です。他のHIF-PH阻害薬(エベレンゾ・エナロイ・マスーレッドの3剤)では「妊婦又は妊娠の可能性のある女性」も禁忌となっていますが、ダーブロックは禁忌ではなく慎重投与の扱いとなっています。これは他剤と異なる点です。
⚠️ 投与中に患者指導すべき血栓症の警告症状
- 片側の手足のしびれ・麻痺(脳梗塞)
- 胸痛・呼吸困難(肺塞栓症・心筋梗塞)
- 突然の視力低下(網膜静脈閉塞)
これらの症状が現れた場合には「速やかに医療機関を受診するよう患者を指導すること」と添付文書に明記されています。患者への説明文書(患者向け資材)も活用してください。
PMDA:ダーブロック錠 患者向け資材「腎性貧血の治療を受けられるみなさまへ」(PDF)
ダーブロック添付文書PDFの用量調節と投与量の段階的設定
用量調節のルールを正確に把握することは、臨床現場における安全管理の要です。
📊 8段階の投与量(添付文書 第7.2項)
| 段階 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
|---|---|---|---|---|---|---|---|---|
| 投与量 | 1mg | 2mg | 4mg | 6mg | 8mg | 12mg | 18mg | 24mg |
1段階ずつ増量または減量する、という原則が重要です。最高用量は1日1回24mgで、これを超えることはできません。
調節後は少なくとも4週間は同一用量を維持することが添付文書に定められています。ただし例外があります。ヘモグロビン濃度が4週以内に2.0g/dLを超えて急激に上昇した場合には、4週を待たずに速やかに減量または休薬が必要です。この急激な上昇は心血管系リスクと関連するため、見逃さないようにしましょう。
🩸 開始用量の決め方(保存期CKD・ESA未治療患者)
| ヘモグロビン濃度 | 開始用量 |
|---|---|
| 9.0g/dL未満 | 4mg(1日1回) |
| 9.0g/dL以上 | 2mg(1日1回) |
ESAから切り替える場合の開始用量は一律4mgです。透析患者(血液透析・腹膜透析)の場合も同様に4mg開始です。
🔍 透析患者のESA切替えで特に注意が必要な点
添付文書8.4項には明確な記載があります。「血液透析患者及び腹膜透析患者において、赤血球造血刺激因子製剤の投与量が高い患者では、本剤への切替え後にヘモグロビン濃度が低下する傾向が認められている」とされており、切替えの必要性を十分検討するよう求められています。切替え後はHb値の推移をこれまで以上に注意深く観察することが必要です。
モニタリングの頻度については、投与開始後はHbが目標範囲で安定するまで2週に1回程度確認し、安定後は4週に1回程度の確認が必要です(添付文書8.1・8.2項)。
PMDA:ダーブロック錠 適正使用ガイド(PDF)— 用量調節の詳細フローチャートを掲載
ダーブロック添付文書PDFの2024年改訂内容:心不全患者への追記
2024年7月の添付文書改訂は、医療従事者が確実に把握しておくべき重要な内容です。
改訂のポイントは「9.1.5 心不全又はその既往歴のある患者」の新規追記です。改訂前の添付文書にはこの項目が存在していませんでした。追記の根拠となったのは、海外臨床試験の事後解析で実施されたサブグループ解析です。
📌 心不全既往患者における心不全入院リスク(海外試験データ)
| 対象 | ダーブロック群 | ESA群 | ハザード比 |
|---|---|---|---|
| 透析期CKD患者 | 17.6%(47/267例) | 12.6%(32/254例) | 1.52(95%CI:0.97–2.38) |
| 保存期CKD患者 | 20.4%(54/265例) | 13.4%(34/254例) | 1.37(95%CI:0.89–2.11) |
両試験ともにダーブロック群で心不全入院の初回発現割合が高い傾向が認められています。95%信頼区間が1をまたいでいるため統計的有意差はないものの、臨床的に無視できないシグナルとして添付文書に反映されました。
心不全またはその既往歴を持つ患者に処方する際は、「心不全が増悪または再発するおそれがある」ことを念頭に置き、定期的な症状確認と必要に応じた中止を考慮する必要があります。この情報は2024年7月以前の添付文書にはなく、古いバージョンを参照している現場では見落とされる可能性があります。最新版を確認するのが必須です。
PMDA:ダプロデュスタットの使用上の注意改訂通知(2024年7月、PDF)— 心不全追記の詳細を掲載
ダーブロック添付文書PDFで確認すべき相互作用とCYP2C8の影響
相互作用の理解は調剤・処方設計において欠かせません。ダーブロックには「併用禁忌」はなく、「併用注意」のみです。ただし、その内容を軽視すると血中濃度が想定外に変動します。
🔄 主な併用注意薬剤(添付文書 第10.2項)
| 薬剤名 | 影響 | 主な機序 |
|---|---|---|
| クロピドグレル(プラビックス等) | 本剤の作用増強 | CYP2C8阻害によりAUCが1.75〜2.65倍に上昇 |
| トリメトプリム | 本剤の作用増強 | AUCが1.48倍、Cmaxが1.28倍に上昇 |
| リファンピシン | 本剤の作用減弱 | CYP2C8誘導により血中濃度が低下 |
CYP2C8阻害作用が問題になります。透析患者ではクロピドグレルを長期服用しているケースが少なくないため、処方チェックが必要です。クロピドグレルを服用中の患者では、Hb値の変動に特に注意してモニタリングを行う必要があります。
一方で食事の影響は軽微である点は、他のHIF-PH阻害薬と比較したダーブロックの特徴です。食後に投与した場合、AUCとCmaxはそれぞれ約9%・11%の低下にとどまります。エナロイ(エナロデュスタット)が空腹時服用指定、マスーレッドが食後服用指定となっているのと対照的で、服薬タイミングの自由度が高い薬剤です。
また、経口鉄剤やリン吸着剤については「ダーブロックの薬物動態に影響を与えなかった」とインタビューフォームに記載されており、他のHIF-PH阻害薬(ロキサデュスタット等)で問題となる多価陽イオンによる吸収阻害をほとんど受けません。透析患者がリン吸着剤と同時に服用する場面でも、時間を空ける必要がない点は実臨床上の利便性に直結します。
ただし、CYP2C8阻害剤との併用では本剤の減量を考慮するよう明記されています。クロピドグレル服用中の患者に対しては、開始時の用量設定と調節に際して一段階低い用量から始めることを検討するのが安全です。
JAPIC:ダーブロック錠 インタビューフォーム(PDF、2025年7月改訂第6版)— 相互作用・調剤情報の詳細を掲載
ダーブロック添付文書PDFで読み解く肝機能・特定背景患者への対応
腎機能だけでなく、肝機能や他の背景因子も添付文書に詳しく記載されています。ここはしばしば見落とされやすい領域です。
🫀 肝機能障害患者(添付文書 9.3項)
軽度肝機能低下者(Child-Pugh分類A)では、Cmaxが1.01倍、AUCが1.46倍に上昇しました。中等度肝機能低下者(Child-Pugh分類B)ではCmaxが1.98倍、AUCが2.00倍と大幅に上昇しています。減量を考慮するとともに慎重な観察が必要です。
重度の肝機能低下者(Child-Pugh分類C)を対象とした臨床試験は実施されていないため、データがない状態での投与は慎重に行う必要があります。
過量投与時の対応についても知っておく必要があります。本剤の血漿蛋白結合率は約99%と非常に高く、血液透析による除去は期待できません。過量投与では減量・休薬等の適切な処置が唯一の対応となります。
他の特定背景患者に関する主な注意事項を整理すると以下のとおりです。
- 悪性腫瘍を合併する患者:血管新生亢進により腫瘍が増悪するおそれがある(9.1.3項)
- 増殖糖尿病網膜症・加齢黄斑変性症等を合併する患者:血管新生亢進により網膜出血があらわれるおそれがある(9.1.4項)
- 高血圧症を合併する患者:血圧上昇があらわれるおそれがある(9.1.2項)
- 妊婦:胎児への移行可能性があるため、有益性が危険性を上回る場合のみ投与可(9.5項)
- 授乳婦:乳汁移行の可能性あり、授乳継続または中止を検討(9.6項)
- 小児:臨床試験未実施のため使用経験なし(9.7項)
高血圧への注意は見落とされやすいポイントです。ダーブロック投与によって血圧が上昇するおそれがあり、血圧の推移に十分注意しながら投与することが8.5項に明記されています。腎性貧血患者の多くはもともと高血圧を合併しているケースが多く、投与開始後の血圧モニタリング強化は実臨床でも重要な意味を持ちます。
ダーブロックはHIF経路を活性化する薬剤であるため、HIF経路を介した血管新生促進の影響が複数の背景疾患で懸念されます。添付文書記載の背景因子を一つひとつ確認する習慣が安全な処方につながります。
日本腎臓学会:HIF-PH阻害薬適正使用に関するRecommendation(PDF)— 特定背景患者の使用判断に役立つガイダンスを掲載
